- Viernes, abril 4, 2025
EL PEZ CEBRA COMO MODELO DE ESTUDIO GENÉTICO
Academia Mexicana de Ciencias
Boletín AMC/126/16
Ciudad de México, 9 de junio de 2016
- Este vertebrado comparte con el ser humano el 70% de información genética y más del 80% de sus genes se relacionan con determinadas enfermedades embrionarias.
- Para el caso del pez cebra no existía ninguna posibilidad de generar mutaciones específicas, pero a partir del surgimiento del sistema de edición genómica CRISPR/Cas9, se ha podido generar mutaciones en distintos genes, lo que permitirá estudiar el papel de esos genes en el desarrollo embrionario o en la fisiología del pez.
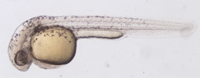
- Embrión de pez cebra (Danio rerio).
Foto: cortesía doctora Lomelí Buyoli.
Galería de imágenes
El entendimiento del control genético durante el desarrollo embrionario es uno de los retos más importantes de la biología moderna. El enfoque de la genética de desarrollo se basa en el uso de tecnologías que permiten la manipulación de genes específicos. En la actualidad se dispone de una gran flexibilidad para la manipulación del genoma de distintas especies animales que han sido utilizadas como modelos de embriogénesis, como el pez cebra, sostuvo Hilda María Lomelí Buyoli, investigadora del Instituto de Biotecnología de la Universidad Nacional Autónoma de México (UNAM).
“Trabajo en genética del desarrollo embrionario desde 1998 y con el pez cebra como modelo a partir del 2008, porque este vertebrado comparte con el ser humano el 70% de información genética y más del 80% de sus genes se relacionan con determinadas enfermedades embrionarias; es decir, conservan genes homólogos que se han identificado en humanos como causantes de enfermedad y esto nos permite, en el pez cebra, generar modelos alterando esos mismos genes y tratando de reproducir la enfermedad”, sostuvo.
Agregó que la ventaja de este pez nativo de India y Pakistán es, que a diferencia de mamíferos como el ratón, puede tener una progenie de miles de individuos, de esta manera los ensayos y los estudios que se hacen tienen valor estadístico mayor:
“La embriogénesis ocurre externamente y los embriones son transparentes, lo que permite observar en el microscopio todos los estadios de su desarrollo, y seguir con detalle las primeras divisiones celulares y la formación de las capas embrionarias. En 24 horas ya se aprecia la segmentación del cerebro y se han formado estructuras como el tubo neural, la notocorda y los somitos (precursores de músculo y esqueleto).
“A las 72 horas ya es una larva desarrollada, y para los cinco días de desarrollo se han formado órganos sensoriales como los ojos y los oídos. Asimismo, han aparecido el corazón, el hígado, los riñones y el páncreas, además de que los sistemas circulatorio, digestivo y nervioso son perfectamente funcionales, esas son ventajas frente a modelos como el ratón, que toma 19 días el proceso de desarrollo embrionario y ocurre en el interior de la madre”, destacó la investigadora del Departamento de Genética del Desarrollo y Fisiología Molecular.
Apuntó que de este vertebrado acuático ya se tiene secuenciado el genoma completo y existen mapas muy precisos de marcadores genéticos. “El interés de nuestro laboratorio se ha centrado en entender el papel de algunos genes característicos de etapas embrionarias. Para ello producimos alteraciones de la expresión genética que nos revelan la importancia de estos genes in vivo”.
Los genes que estudia la doctora y su equipo de trabajo incluyen a la familia de los genes Zimp: Zimp7 y Zimp10; y a los genes Arid: Arid1a y Arid1b. Los homólogos de los genes Zimp y Arid se identificaron inicialmente en Drosophila melanogaster (mosca de la fruta).
Una nueva técnica
Antes de que existiera el sistema de edición genómica CRISPR/Cas9, para el caso del pez cebra no existía ninguna posibilidad de generar mutaciones específicas; es decir, se podían generar mutaciones de forma global, apagar la expresión de un gen inyectando alguna molécula que obstruyera su actividad por un tiempo corto, pero no se estaba en posibilidad de generar una mutación específica en una línea estable y “a partir del surgimiento de esta técnica hemos podido generar mutaciones en distintos genes y eso representa un gran avance, porque solo así podemos realmente estudiar el papel de esos genes en el desarrollo embrionario o en la fisiología del pez”.
De acuerdo con Hilda María Lomelí Buyoli, quien trabaja con la técnica CRISPR desde hace dos años en su laboratorio, este tipo de estudios en el pez cebra son fundamentales para preguntarse en general cómo ocurre el desarrollo embrionario, debido a que su interés se centra en conocer de qué manera los genes determinan la formación de órganos, su totipotencialidad, y la diferenciación, preguntas del desarrollo embrionario muy generales que además tienen consecuencias en la biomedicina.
Elizabeth Ruiz Jaimes.
Regresar Arriba, o a Comunicados, o al Inicio.
AMC "Casa Tlalpan" Calle Cipreses s/n, km 23.5 de la carretera federal México - Cuernavaca, San
Andrés Totoltepec, Tlalpan, C.P. 14400, México, D.F.
Coordinación de Comunicación y Divulgación
Teléfonos: (52-55) 58 49 49 04, Fax: (52-55) 58 49 51 10, amcpress@unam.mx
Mapa de ubicación
